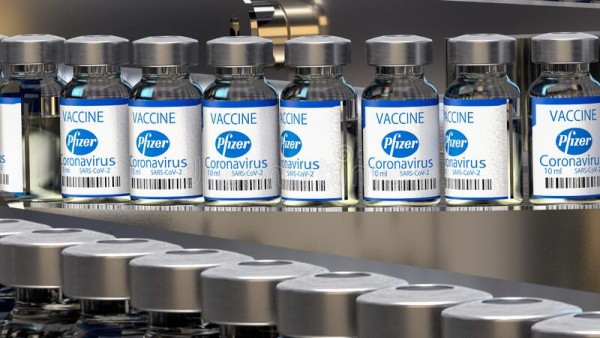
En las 11 semanas que terminaron el 15 de diciembre los estantes de las farmacias en Estados Unidos se llenaron de vacunas sin usar, ya que millones se infectaron con Covid-19 y en este lapso murieron 100 mil personas, casi todas no vacunadas. Foto: https://www.dreamstime.com.
Marco Vinicio González
Ante la llegada de nuevas variants del COVID-19 la Administracion de Medicinas y Alimentos, FDA, autorizó las vacunas bivalentes de Moderna y Pfizer-BioNTech para su uso como dosis de refuerzo actualizadas, dirigidas a las subvariantes de Omicrom que actualmente son dominantes, para tartar de evitar un repentino rebrote del virus en el otoño o el invierno, tradicional época de la gripa que nuevas subvariantes del virus puedan aprovechar para ‘viajar de mosca’ y hacer más complicado el escenario.
Se trata del primer rediseño de una vacuna contra el coronavirus desde que estuvo disponible por primera vez hace casi dos años, y podría estar disponibles la próxima semana, dice la FDA.
Estas nuevas vacunas bivalentes contienen dos componentes de ARN que sirven, uno, como “mensajero (ARNm) de la cepa original del SARS-CoV-2, y el otro, más común entre las variantes omicron BA.4 y BA.5”.
La vacuna bivalente de Moderna está autorizada para su uso como dosis de refuerzo única en personas de 18 años y mayores. Y la de Pfizer-BioNTech para su uso como dosis única de refuerzo en personas de 12 años de edad en adelante.
Por su parte,la Secretaría de Salud de la administración Biden afirman que incluso mientras los investigadores trabajan para comprender qué tan eficaces podrían ser estas nuevas vacunas, “inocular a los estadunidenses otra vez en las próximas semanas podría ayudar a frenar la cantidad persistentemente alta de infecciones y muertes”, que se han vuelto a ver últimamente con el repunte de las variants y sus subvariantes, cada vez más agresivamente contagiosas.
Qué incluyen las vacunas bivalentes o refuerzos actualizados:
- Un componente de ARNm de la cepa original para proporcionar una respuesta inmune
- Un componente de ARNm común entre la BA.4 y BA.5 que actualmente causan la mayoría de los casos de COVID-19 en Estados Unidos.
- Se prevé que circulen este otoño e invierno.
- Decisión basada en la totalidad de la evidencia disponible.
- Datos extensos de seguridad y eficacia.
- Datos de seguridad e inmunogenicidad, de un estudio clínico de vacuna bivalente contra el covid.
Según los datos que respaldan cada una de estas autorizaciones, se espera que las vacunas bivalentes contra el COVID-19 brinden una mayor protección contra la variante omicron que circula actualmente. Las personas que reciben una vacuna COVID-19 bivalente pueden experimentar efectos secundarios comunes a los de las personas que reciben vacunas aprobadas de COVID-19 de ARNm monovalentes.
Con todo, desde hoy las vacunas monovalentes de ARNm contra el COVID-19 no están ya autorizadas como dosis de refuerzo para personas mayores de 12 años.
¿Quién es elegible para recibir una nueva dosis única de refuerzo y cuándo?
- Personas mayores de 18 años si han pasado al menos dos meses desde que recibieron la más reciente dosis de refuerzo con cualquier vacuna monovalente COVID-19 autorizada.
- Personas de 12 años de edad y mayores, elegibles para una sola dosis de refuerzo de la vacuna bivalente de Pfizer-BioNTech COVID-19 si han pasado al menos dos meses desde que completaron la vacunación primaria, o la dosis de refuerzo con cualquier vacuna autorizada•